Das erste Isotop, das zu dieser Liste gehört, ist das Kalium mit der Ordnungszahl 19. Es wird hier, wie auch in späteren Analysen als Codierungszahl separat behandelt und steht in der Kopfzeile. Es folgen nach dem Kalium genau 2 x 19 Isotope, die 28 verschiedenen Elementen angehören. Die besondere Zahl 19, die hier hervortritt, regiert das System der Isotope maßgeblich.
Die 43 und 61 im System der Elemente
Insgesamt gibt es 61 Elemente, bei denen die Neutronen-Überzahl größer als 1 ist (Ordnungszahlen 21 bis 83 minus die beiden Elemente 43 und 61). Die größte Neutronen-Überzahl 43 finden wir bei Wismut, dem letzten der stabilen Elemente. Das bedeutet, dass bereits in den Differenz-Zahlen ein Teil des Bauplans des Elemente-Systems sichtbar wird. Die Art und Weise, wie der Bauplan in diesem Fall beschrieben wird, zeigt aber auch, dass es sich nicht um eine physikalische Gesetzmäßigkeit handelt, sondern um eine Designer-Maßnahme (oder einen weiteren Zufall, worauf gewisse Kritiker sicherlich bestehen werden).
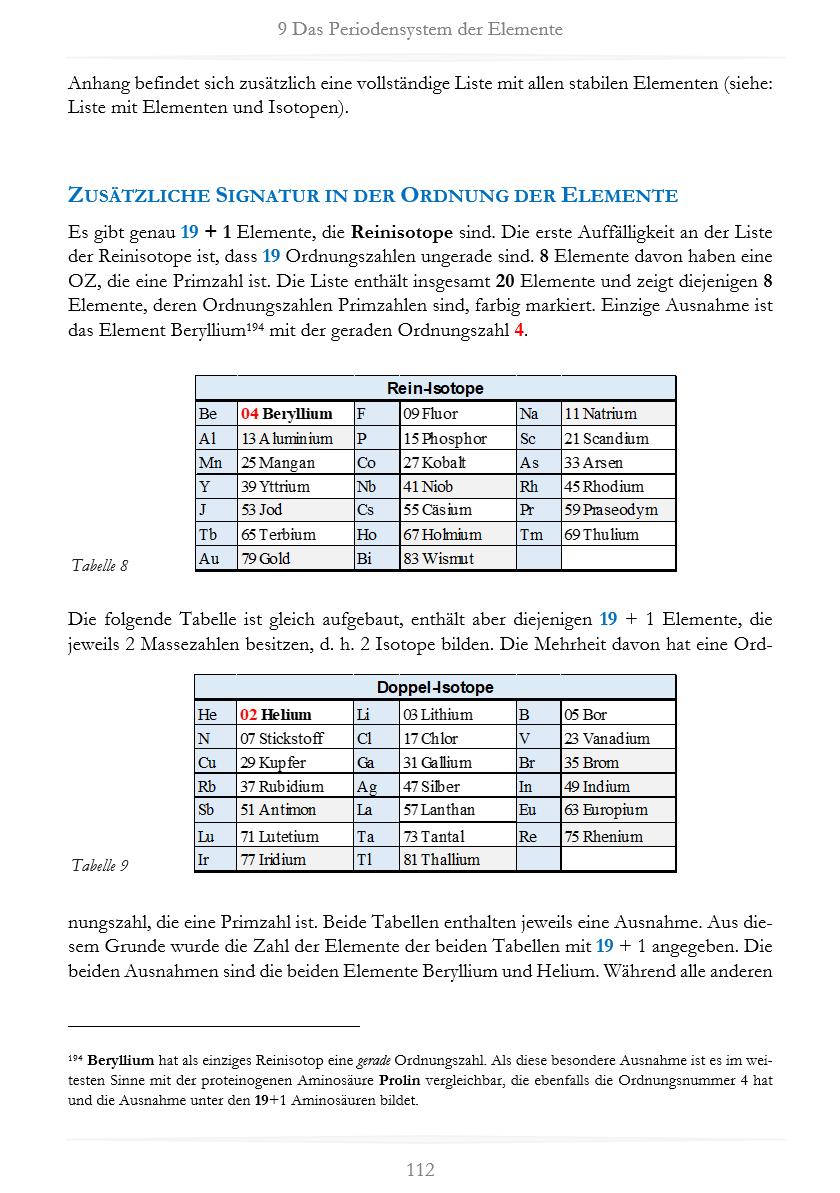
Einige Elemente kommen als Rein-Isotop vor. Das bedeutet, dass es von diesen Elementen in der Natur jeweils nur eine Form gibt. Das Element Fluor mit der Ordnungszahl 9 ist zum Beispiel ein Reinisotop. Es hat 9 Protonen und 10 Neutronen im Kern und somit eine Massezahl von 19. Zwar wurden auch von diesem Atom eine Reihe künstlich herstellbare Isotope entdeckt, die jedoch alle nur für sehr kurze Zeit existieren, also nicht in der Natur vorkommen können.
Neben den Reinisotopen gibt es Elemente, die man als Doppel-Isotope bezeichnen kann. Sie kommen in genau 2 verschiedenen Formen stabil vor. Analog dazu gibt es Elemente, die man als Mehrfach-Isotope bezeichnen kann, weil sie in der Natur mit mehr als 2 stabilen Isotopen vorkommen. Die Anzahl der stabilen Isotope zu einem Element reicht von 1 bis 10. Addiert man alle stabilen Isotope, so erhält man 283, was die 61. Primzahl ist, wenn man die 2 als erste Primzahl bezeichnet.
Diese Unterscheidung der Elemente nach ihrer Anzahl Isotope ist die Grundlage für die weitere Analyse. Wir möchten uns auch noch einmal klar machen, dass die folgenden Untersuchungsergebnisse ebenfalls keine naturgesetzlichen Notwendigkeiten sind, wie zum Beispiel die Gesetze, die das chemische oder physikalische Verhalten und Eigenschaften der Elemente betreffen. Es ist wichtig, das im Sinn zu behalten, weil eine Signatur des Schöpfers viel besser wahrgenommen werden kann, wenn sie nicht gleichzeitig grundlegenden Eigenschaften der Elemente beschreibt. Falls jemand in der Methode, wie wir die Atome zu Gruppen zusammenfassen, einen esoterischen Ansatz vermutet, wie das von einzelnen Kritikern tatsächlich schon unterstellt wurde, so sei ihm empfohlen, dieses Kapitel von Anfang an noch einmal Schritt für Schritt zu lesen und gründlicher zu prüfen. Im Anhang befindet sich zusätzlich eine vollständige Liste mit allen stabilen Elementen (siehe: Liste mit Elementen und Isotopen).
Die 43 und 61 im System der Elemente
Insgesamt gibt es 61 Elemente, bei denen die Neutronen-Überzahl größer als 1 ist (Ordnungszahlen 21 bis 83 minus die beiden Elemente 43 und 61). Die größte Neutronen-Überzahl 43 finden wir bei Wismut, dem letzten der stabilen Elemente. Das bedeutet, dass bereits in den Differenz-Zahlen ein Teil des Bauplans des Elemente-Systems sichtbar wird. Die Art und Weise, wie der Bauplan in diesem Fall beschrieben wird, zeigt aber auch, dass es sich nicht um eine physikalische Gesetzmäßigkeit handelt, sondern um eine Designer-Maßnahme (oder einen weiteren Zufall, worauf gewisse Kritiker sicherlich bestehen werden).
Einige Elemente kommen als Rein-Isotop vor. Das bedeutet, dass es von diesen Elementen in der Natur jeweils nur eine Form gibt. Das Element Fluor mit der Ordnungszahl 9 ist zum Beispiel ein Reinisotop. Es hat 9 Protonen und 10 Neutronen im Kern und somit eine Massezahl von 19. Zwar wurden auch von diesem Atom eine Reihe künstlich herstellbare Isotope entdeckt, die jedoch alle nur für sehr kurze Zeit existieren, also nicht in der Natur vorkommen können.
Neben den Reinisotopen gibt es Elemente, die man als Doppel-Isotope bezeichnen kann. Sie kommen in genau 2 verschiedenen Formen stabil vor. Analog dazu gibt es Elemente, die man als Mehrfach-Isotope bezeichnen kann, weil sie in der Natur mit mehr als 2 stabilen Isotopen vorkommen. Die Anzahl der stabilen Isotope zu einem Element reicht von 1 bis 10. Addiert man alle stabilen Isotope, so erhält man 283, was die 61. Primzahl ist, wenn man die 2 als erste Primzahl bezeichnet.
Diese Unterscheidung der Elemente nach ihrer Anzahl Isotope ist die Grundlage für die weitere Analyse. Wir möchten uns auch noch einmal klar machen, dass die folgenden Untersuchungsergebnisse ebenfalls keine naturgesetzlichen Notwendigkeiten sind, wie zum Beispiel die Gesetze, die das chemische oder physikalische Verhalten und Eigenschaften der Elemente betreffen. Es ist wichtig, das im Sinn zu behalten, weil eine Signatur des Schöpfers viel besser wahrgenommen werden kann, wenn sie nicht gleichzeitig grundlegenden Eigenschaften der Elemente beschreibt. Falls jemand in der Methode, wie wir die Atome zu Gruppen zusammenfassen, einen esoterischen Ansatz vermutet, wie das von einzelnen Kritikern tatsächlich schon unterstellt wurde, so sei ihm empfohlen, dieses Kapitel von Anfang an noch einmal Schritt für Schritt zu lesen und gründlicher zu prüfen. Im Anhang befindet sich zusätzlich eine vollständige Liste mit allen stabilen Elementen (siehe: Liste mit Elementen und Isotopen).

Leseprobe 2